ANMDM: „Nu s-au identificat reacții adverse pentru HEXAXIM”
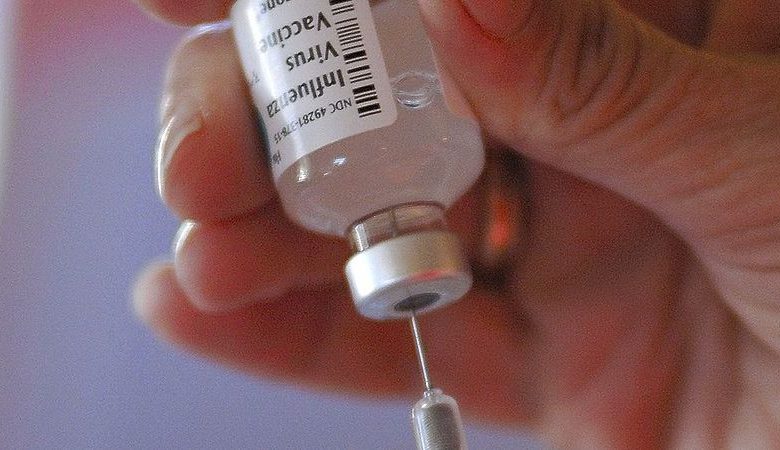
Cu puțin timp în urmă, Agenția Națională a Medicamentului și a Dispozitivelor Medicale (ANMDM) a adus precizări cu privire la legalitatea emiterii de către autoritate pentru furnizarea de medicamente pentru nevoi speciale pentru vaccinul hexavalent HEXAXIM, utilizat în Programul național de vaccinare.
Amintim că în raportul Corpului de control al premierului, publicat miercuri, au fost menționate neregulile depistate în cazul gestionării crizei bebelușilor bolnavi, după o investigație la Spitalul de copii din Argeș și la Spitalul de Copii „Marie Curie”. Dar, concluzille raportului sunt contrazise de Agenţia Naţională a Medicamentului.
Astfel, Corpul de control al premierului a solicitat Parchetului de pe lângă Înalta Curte de Casaţie şi Justiţie (PÎCCJ) verificări privind stocurile de vaccinuri existente la nivelul Direcţiilor judeţene de sănătate publică, a spitalelor şi a cabinetelor medicale. Mai exact, trebuie verificată calitatea vaccinurilor.
citește și: Guvernul cere verificarea vaccinurilor, după îmbolnăvirea copiilor din Argeş
Așadar, ANMDM aduce argumente cu privire la vaccinul incriminat, HEXAXIM, despre care spune că este autorizat conform legii. Corpul de control anunțase că vaccinul destinat pieței din Kazahstan ar fi fost aprobat incorect, prin omiterea unor pași obligatorii
Pe site-ul institutului a fost postat un comunicat cu detalii despre cum a fost achiziționat acest vaccin.
„Reiterăm faptul că discontinuitatea în aprovizionare cu vaccinul Hexacima al producătorului Sanofi Pasteur a impus, în decembrie 2015, ca măsură de protecție a sănătății publice, asigurarea disponibilității prin pârghia legislativă a autorizației pentru nevoi speciale, a vaccinului Hexaxim al aceluiași producător (un număr de 107.300 doze vaccin), după modelul și al altor state membre UE (cazul Belgiei, Poloniei de exemplu). Scopul acestor proceduri a fost acela de a asigura continuitatea programelor naționale de imunizare, cu respectarea criteriilor riguroase privind autorizarea”.
„Hexaxim a fost evaluat de Agenția Europeană a Medicamentului (EMA), care a emis în acest sens o opinie științifică pozitivă, EMA garantând cu privire la echivalenta standardelor de evaluare a documentației de autorizare pentru produsele Hexacima/Hexyon/Hexaxim.”
mai multe aflați de aici: Comunicat ANMDM referitor la HEXAXIM
Acest material este proprietatea site-ului Mytex.ro si poate fi preluat pe site-ul dvs doar cu citarea sursei prin afisarea linkului catre articolul din site-ul mytex.